结直肠癌是一种常见的消化道恶性肿瘤,其发病率与死亡率在所有癌症中均处于前三位,严重威胁到人类健康。肠道靶向递送载体的出现为临床治疗结直肠癌提供了新的思路,其中通过消化道给药能够将药物有效成分直接递送到肿瘤发病部位,是一种理想的靶向结直肠癌的给药方式。但是一些常规的药物载体难以穿透肠屏障且容易在肠道内降解并被排出体外。因此,研发一种结构稳定、生物相容性好、能够适应消化道环境的药物载体是临床上亟待解决的问题。近日,中国农业大学、北京食品营养与人类健康高精尖创新中心的于政权和李媛研究小组在生物医学1区杂志《Theranostics》上发表封面文章(Theranostics,2020,10,3594-3611. IF: 8.651),报道了一种由食品级乳清蛋白和氧化魔芋多糖为原料的肠靶向递送体系,具有良好的肠道靶向性和生物相容性,能够通过口服或直肠给药的方式将抗肿瘤核酸药物和姜黄素递送到直肠部位,并在动物模型中有效地抑制了肿瘤的生长,为临床治疗直肠癌提供了新的治疗策略。

本研究首先利用α-乳清白蛋白水解后得到的多肽通过自组装形成粒径约20 nm左右的球形纳米颗粒 (Peptosomes, PS)。其疏水性内核能够包裹脂溶性姜黄素,正电荷外壳则可以吸附microRNA-31抑制剂。同时将能够特异性识别结直肠肿瘤表面分子标记物CD133的靶向肽连接到α-乳清白蛋白纳米颗粒上,从而成功构建了一个能够靶向结直肠癌递送并同时携带两种药物的PS纳米药物。
为了使纳米药物能够通过消化道给药方式进行递送并在体内保持稳定,本研究进一步将氧化魔芋多糖进行双交联使其形成微球体 (Oxidized Konjac Glucomannan microsphere, sOKGM),并在此过程中将PS纳米药物包裹在微球体中,构建了一个能够通过消化道进行递送并靶向结直肠癌的α-乳清白蛋白纳米颗粒-氧化魔芋多糖微球体复合递送体系 (sOKGM-PS)。
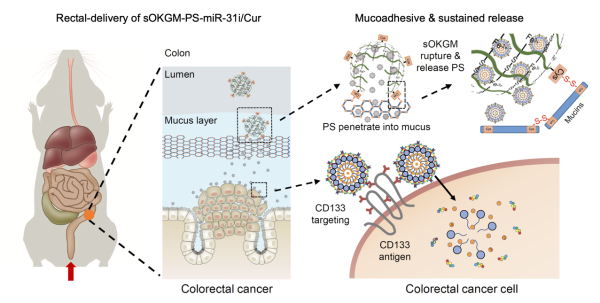
sOKGM-PS载药体系具有良好的生物相容性和理化稳定性,能够在胃肠环境中长时间保持结构稳定,同时可以对其内部的PS纳米药物进行缓慢释放。sOKGM-PS可以通过口服或直肠给药的方式在体内进行递送到达结直肠部位并对结肠粘液层具有黏附作用,其缓慢释放出的PS纳米药物则能够利用自身体积微小的优势有效通过肠屏障,进一步通过靶向肽识别肿瘤细胞并将其携带的抗肿瘤成分microRNA-31抑制剂和姜黄素释放到肿瘤细胞中。最终,sOKGM-PS载药体系可以有效缓解AOM-DSS诱导的结直肠癌模型小鼠中肿瘤的生长。
本研究利用α-乳清白蛋白纳米颗粒和氧化魔芋多糖微球体成功构建了一个抗肿瘤纳米药物载药体系,通过体外和体内实验证明了其能够有效地通过消化道给药途径将microRNA-31抑制剂和姜黄素靶向递送到结直肠肿瘤组织中并抑制肿瘤的生长。本研究有效解决了microRNA制剂无法在体内稳定存在以及纳米药物难以高效递送至结直肠肿瘤组织中的难题,为临床治疗结直肠癌提供了新的治疗策略。
中国农业大学、北京食品营养与人类健康高精尖创新中心的于政权和李媛教授为文章的共同通讯作者,课题组成员赵然和杜素娟为文章的并列第一作者。
参考文献:
Zhao R, Du S, Liu Y, Lv C, Song Y, Chen X, Zhang B, Li D, Gao S, Cui W, Plikus MV, Hou X, Wu K, Liu Z, Liu Z, Cong Y, Li Y*, Yu Z*. Mucoadhesive-to-penetrating controllable peptosomes-in-microspheres co-loaded with anti-miR-31 oligonucleotide and Curcumin for targeted colorectal cancer therapy. Theranostics 2020; 10(8):3594-3611.
原文链接:https://www.thno.org/v10p3594.htm